Os hidrocarbonetos naturais são compostos químicos constituídos por átomos de carbono e de hidrogénio.
As diferentes características físicas são uma consequência das diferentes composições moleculares.
Contudo, todos os hidrocarbonetos apresentam uma propriedade comum: "ardem", isto é, oxidam-se facilmente libertando calor (são combustíveis).
Os hidrocarbonetos são constituídos, como já referimos, por átomos de carbono e de hidrogénio. São as diferentes ligações químicas entre os carbonos (covalente simples, dupla ou tripla) que determinam se pertencem ao grupo dos alcanos, dos alcenos, ou dos alcinos, respectivamente.
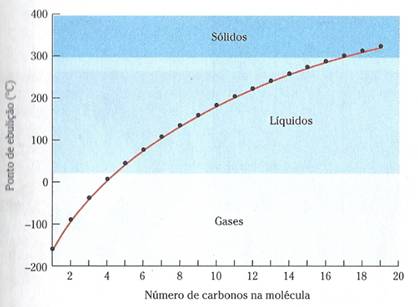
(Gráfico 1 - relação do ponto de ebulição com o número de átomos de carbono num hidrocarboneto)
Como podemos constatar através da análise do gráfico acima evidenciado:
· Os hidrocarbonetos com moléculas mais simples e leves (metano, etano, propano, butano) são gasosos à temperatura ambiente e pressão normal.
· Os hidrocarbonetos mais pesados (com maior número de carbonos) são sólidos às condições referidas na alínea anterior.
· Aqueles que se encontram entre estes dois grupos, encontram-se no estado líquido, em condições naturais.
Isto significa que é o aumento do número de carbonos (ou seja, se a molécula é mais pesada ou não) que faz com que o seu ponto de ebulição aumente.
